


Laboratory for
Epigenome Inheritance
RIKEN IMS, Yokohama, Japan
世代をつなぐ 受精卵を科学する
親の形質はDNAを介して子供に伝わります。その情報伝達を担うのが配偶子(卵と精子)です。配偶子には、DNAだけでなく、その取扱説明書にあたる「エピゲノム」情報も含まれています。受精後にエピゲノムがDNAと一緒に伝承されることで、次世代個体が正常に形作られます。当研究室は、親世代での配偶子が作られる過程でどのようにエピゲノムが正確に作り出され、それがどのようにして次世代へと伝承され、どのように働くかについて研究しています。さらに、親世代の環境要因がエピゲノムの世代間伝承に影響するかを検証します。この研究は、ラマルクが提唱した獲得形質の遺伝を最新の科学技術で再検証する試みとも捉えられます。このために当研究室では、主にマウスをモデルに用いて、(1) 卵形成過程におけるエピゲノム確立機構と次世代への伝承機構、(2) エピゲノム伝承の意義、(3) 伝承性エピゲノムを介した疾患素因の形成機構、などの研究を行っています。これらの研究を通じて、配偶子形成や受精直後の分子の振る舞いが、その後の胎児の発生や子の形質・体質に長期的な影響を及ぼす分子基盤を解明します。
キーワード: エピジェネティクス、ヒストン、ゲノム刷り込み、卵、着床前初期胚、胎盤
現在進行中の研究テーマ
1. 卵母細胞におけるエピゲノム確立機構と次世代への伝承機構
2. ヒストンによるエピゲノム伝承の意義
3. 母性環境や疾患によるエピゲノム伝承への作用
「世代を超えるエピゲノム〜生殖細胞による獲得形質の遺伝を再考する〜」
実験医学 2021年 4月号 39(6): 856-61、羊土社
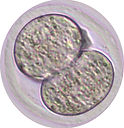
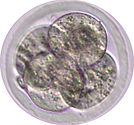
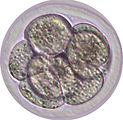
着床前初期胚
新しい命は受精から始まります。精子と卵子という性質の全く異なる二つの細胞が融合して、受精卵ができます。受精卵は、次世代個体を構成する全ての細胞の源です。受精卵は卵割を繰り返し、2細胞期胚、4細胞期胚、8-16細胞の桑実胚、32細胞以上の胚盤胞期胚となります。この発生過程は、卵管および子宮内において着床以前に起こるため、着床前発生と呼ばれます。配偶子形成から着床前発生の過程においてはエピゲノムの大規模な変化が起こるため(後述)、エピゲノム研究に優れた実験モデルとなります。研究モデルとして着床前胚の優れた点は、容易に体外に取り出して培養することができて、再び体内に戻すと個体を誕生させられることです。このようなex vivoの実験系により、生体内に限りなく近い生理的な条件において、実験的介入(CRISPRによるゲノム編集、RNAiによる遺伝子機能抑制、mRNA注入による外来遺伝子の発現誘導など)が容易に行えます。


エピジェネティクス
いまさらですがエピジェネティクス(=エピゲノム)とは何でしょうか。細胞の核内において、実はDNAは裸でフラフラしているわけではなく、DNAはヒストンという塩基性に富んだ小さなタンパク質に巻きついて、数珠のような形で収納されています。このような構造体をクロマチンといいます。細胞は、ヒストンを有効活用することで、遺伝子の発現を制御しています。例えば、ヒストンにメチル化、アセチル化、ユビキチン化、リン酸化といった翻訳後修飾を付加することで、クロマチンは緩んだり閉じたりします。その結果、転写マシーナリーのDNAへの結合を促進あるいは阻害されます。また、DNA自体もメチル化などの化学修飾を受けます。このようにクロマチンへの化学修飾を介して遺伝子発現を制御するシステムを「エピゲノム制御」、化学修飾を「エピゲノム修飾」などと呼びます。よく用いられる好例が「付箋」です。分厚い本に相当するゲノムに対して、エピジェネティクスはどのページを読むかという付箋の役割を果たします(下図左)。ちなみに、さらにそのページのどの文を読むかを指示するのが転写因子の役割だと私は理解していますが(下図右)、転写因子がエピジェネティクスの上流にあることもあります。エピゲノムのパターン(付箋の位置)はそれぞれの細胞種に特有であるため、細胞種に特有の遺伝子発現プログラムが可能になります。エピジェネティクス研究の歴史や詳細について知りたい方はコチラ(外部サイト)。


エピゲノムリプログラミング
精子と卵子が形成される配偶子形成過程で、それぞれ独自のエピゲノムを確立します。そのため、これらのエピゲノム状態はまったく異なります。それらが融合(受精)するので、一つの受精卵において、精子由来の父性染色体と卵子由来の母性染色体の間ではエピゲノムが非対称な状態で存在します。この非対称性は、着床前初期発生の過程で初期化(リプログラミング)されることで解消します。つまり、一旦真っ白なキャンバスに戻すことで、着床後の分化に伴う新たなエピゲノム情報(胚性エピゲノム)を書き込むことを可能にする、というわけです。

リプログラミング抵抗性とインプリンティング
着床前胚におけるエピゲノムの初期化は大規模に起こりますが、実はそれを乗り越えるゲノム領域も存在します。このようなリプログラミング抵抗性の領域は、父母染色体間のエピゲノムが異なったままの状態で発生していくため、父性あるいは母性染色体に特異的な遺伝子発現が起こります。このような片親性の発現をする遺伝子は刷り込み遺伝子と呼ばれ、これまで100個ほど同定されています。ゲノム刷り込み(インプリンティング)を制御するのが、DNAのメチル化です。精子と卵子間で異なるDNAメチル化を示すゲノム領域の一部は、リプログラミングを免れて、次世代に伝承され、刷り込み発現を引き起こします。ヒトにおいて刷り込みの破綻は重篤な疾患を引き起こすため、インプリンティングの制御機構の理解は重要です。ゲノム刷り込みの発見の業績で、2025年にはAzim Surani博士が京都賞を受賞しました。

新しいインプリンティング機構
1991年に哺乳類の刷り込み遺伝子が同定されて以降、配偶子から次世代に経世代伝承される修飾として唯一知られていたのがDNAメチル化でした。しかし、DNAメチル化を無くしても父性アレル特異的発現を示す刷り込み遺伝子が複数同定されており、DNAメチル化以外の刷り込み修飾が存在することが示唆されていました。
受精卵におけるエピゲノムのリプログラミング機構を研究していた我々は、この刷り込み修飾がH3K27me3(ヒストンH3リジン27のトリメチル化)であることを発見しました(Inoue et al., 2017 Nature)。卵のH3K27me3は受精後に母性染色体だけで維持されて、その遺伝子発現を抑制することで刷り込み発現を制御していました。この新たな刷り込み機構は、X染色体不活性化のマスターレギュレーターであるXist遺伝子も制御しており、マウスの着床前胚および胎盤における刷り込み型X染色体不活性化機構の解明につながりました(Inoue et al., 2017 Genes Dev; Inoue et al., 2018 Genes Dev)。今では、DNAメチル化による刷り込みは「典型インプリンティング」、母性H3K27me3による刷り込み機構は「非典型インプリンティング」という名称で定着しており、H3K27me3はDNAメチル化に次ぐ第二の経世代エピゲノムとして位置付けられています。
その後も我々は、非典型インプリンティングの破綻モデルマウスを作製し、この胚が着床後に半数以上が致死に至ることや、出生に至った個体においては胎盤が過形成することなどを見出しました(Inoue et al., 2018 Genes Dev, Mei et al., 2021 Nat Genet)。そして、胚発生および胎盤形成に重要な役割を果たす複数の非典型インプリンティング遺伝子を特定しました(Matoba, Kozuka et al., 2022 Genes Dev)。非典型インプリンティングは、 着床後には胎盤を含む胚体外の細胞系譜において長期維持されますが、なぜ細胞系列特異的なのか、なぜDNAメチル化ではなくヒストンで制御される必要があるのか、Xist以外の非典型インプリンティングの機能は何か、など、多くの未解決な疑問が残っています。

代表的な成果1
H2AK119ub1 guides maternal inheritance and zygotic deposition of H3K27me3 in mouse embryos (Mei et a., 2021 Nat Genet)
H3K27me3が卵の形成過程でどのように確立され、どのように次世代に伝承されるのかを調べるために、H3K27me3と相互作用するヒストンH2Aリジン119モノユビキチン化修飾(H2AK119ub1)に着目し、その役割を調べました。微量CUT&RUN法を用いて、卵成長過程と着床前発生過程でのH2AK119ub1の挙動を調べたところ、卵成長過程においてはH2AK119ub1とH3K27me3は広く共局在することが分かりました。一方で、受精後はこれらの修飾は異なる挙動を示し、典型的なポリコーム抑制複合体の標的である発生関連遺伝子群においては、H2AK119ub1がH3K27me3に先立って確立されることが分かりました。これは、生体内においてH2AK119ub1がH3K27me3をガイドする様子を捉えた初めての報告です。
続いて卵形成過程においてH2AK119ub1がH3K27me3の確立に必要かどうかを調べるために、異型ポリコーム抑制複合体1 (PRC1)の必須構成因子であるpolycomb group ring finger 1 (PCGF1)とPCGF6を欠損させた卵を作成しました。異型PRC1欠損卵ではH2AK119ub1はゲノムワイドに減少し、約2,000個の遺伝子においてH3K27me3の確立不全が起こりました。野生型の精子と受精させて得られた異型PRC1母方欠損胚のH3K27me3の分布を詳細に調べたところ、卵においてH3K27me3を確立できなかった遺伝子群は、受精後もH3K27me3が欠落したままの状態で発生することが分かりました(下図A)。そして着床後に、非典型刷り込み(ヒストン型インプリンティング)の破綻(下図B)、着床後の胎生部分致死、および、出生に至った個体において胎盤が過形成することなどを見出しました(下図C)。つまり、卵形成過程でH3K27me3の刷り込みに失敗すると、その後にH3K27me3修飾酵素が存在していても、もはや取り返しが付かないのです。そして、胎盤過形成という表現型は、母が卵のヒストン修飾を介して胎盤のサイズを抑制すると解釈することができますが、これはヒストン型インプリンティングが「綱引き仮説(インプリンティングの進化理論の一つで、コンフリクト仮説とも呼ばれる)」を支持することを意味します。このように、ポリコーム分子生物学とゲノム刷り込みの面白さが濃縮した論文となりました。

代表的な成果2
H3K27 di-methylation dynamics reveal stepwise establishment of facultative heterochromatin in early mouse embryos (Matsuwaka et al., 2025 Nat Cell Biol)
上述のように、卵子から初期胚に伝わるH3K27me3ドメインは非典型刷り込みを制御します。その一方で、ポリコームの典型的な標的である “発生関連遺伝子群”のプロモーター領域においては、初期発生過程で新たにH3K27me3修飾が確立します。発生関連遺伝子群は分化や器官形成に重要な数千個の遺伝子からなり、ポリコームによるその精巧な発現制御は発生に不可欠です。さらに、初期発生過程では父性X染色体不活性化(XCI)が起こり、H3K27me3がX染色体に新規に確立されます。しかし、これらの領域におけるH3K27me3の新規確立がどのようなメカニズムで起こっているのかは不明でした。
この謎を解くために、本研究ではH3K27me3の前駆体である“H3K27me2”の初期発生動態を微量CATCH-seq法を用いて明らかにしました。そしてH2AK119ub1とH3K27me3との詳細な統合解析の結果、発生関連遺伝子群やX染色体において、最初にH2AK119ub1が確立され、続いて桑実胚期にH3K27me2が確立、そして最後に胚盤胞期にH3K27me3が確立されることを見出しました。
続いてH3K27me2の確立を担う因子を同定するために、PRC2を構成するさまざまなサブユニットの遺伝子発現量を調べたところ、PRC2のサブタイプの一つであるPRC2.2を構成するアクセサリーサブユニットの“JARID2”の発現量が8細胞期以降で大きく上昇していることが分かりました。さらに微量CUT&RUN法を用いて、桑実胚においてJARID2とSUZ12(PRC2のコアサブユニット)は発生関連遺伝子群やX染色体に共蓄積していることが分かりました。そして、Jarid2 KO胚を詳細に解析することで、JARID2が発生関連遺伝子群やX染色体へのSUZ12の結合とH3K27me2(桑実胚期)およびH3K27me3(胚盤胞期)の確立に必須であることが分かりました。JARID2はH2AK119ub1への結合活性を有するため、H2Aub→JARID2-PRC2.2→H3K27me2→H3K27me3という段階的な経路でH3K27me3が新規確立されることが強く示唆されました(下図)。これは発生最初期にエピゲノムがどのように構築されるかを解明した重要な成果です。

特色ある研究手法
一般的な分子生物学・遺伝学ツールの他に、当研究室では以下の3つの特徴的な研究手法を用いています。これらを統合できる研究室は世界的にも稀であり、国際的に高い優位性を発揮できています。コラボレーションの依頼はお気軽に相談ください。
1. 微量エピゲノム解析技術
- Carrier-assisted ChIP-seq (CATCH-seq) (Matsuwaka et al., 2025 Nat Cell Biol; Mei et al., 2025 NSMB, Mei et al., 2026 Mol Cell)
- 微量DNaseI-seq (Lu et al., 2016 Cell; Inoue et al., 2017 Nature)
- 微量CUT&RUN (Hayashi and Inoue, 2022 Method Mol Biol)
- 微量RRBS (DNAメチローム)(Shen et al., 2014 CSC, Inoue et al., 2015 Cell Rep)

2. 顕微操作&生殖工学技術
mRNA/siRNA顕微注入、前核単離、前核置換、染色体置換、体細胞核移植、体外受精、体外成熟培養、体外成長培養、顕微授精、卵管胚移植、子宮胚移植、E6.5胚の3胚葉単離、など
3. 母性因子ノックダウンシステム
3-1. GV卵インジェクション→体外成熟→体外受精
受精前後に起こるほとんどのイベントは卵に蓄えられたタンパク質(母性因子)で制御されています。そのため、この時期の現象のメカニズムや機能の研究には母性因子の機能欠損アプローチが必要です。その方法の一つに卵特異的ノックアウトマウスがありますが、作成に長期間かかりコストも非常に高いのでスループットが上げられません。そこでRNA干渉(siRNAなど)を用いたノックダウンがよく用いられますが、ここに受精卵研究特有の難しさがあります。というのも、卵はその成長過程で多量のタンパク質を貯蓄しているため、siRNAをMII卵に顕微注入しても「時すでに遅し」で、受精までの短時間でターゲット遺伝子をタンパク質レベルでノックダウンできることは稀です。そこで我々は、siRNAをGV卵に顕微注入し、体外成熟の後に体外受精するアプローチを使用しています。これによりsiRNA注入後にGV期を最大24時間維持させ、その後の18時間の体外成熟を合わせて、合計最大42時間の猶予を受精前に与えることで、比較的安定なタンパク質でもノックダウンすることができます。この方法は過去に、Tet3やNfyaなどの母性因子に対して用いました(Inoue et al., 2012 Cell Res; Lu et al., 2016 Cell)。
3-2. 二次卵胞インジェクション
GV卵インジェクションを用いても、比較的安定な母性タンパク質はノックダウンできないことがしばしばあります。この問題を解決するために、二次卵胞インジェクション法を用いています(Inoue et al., 2014 Protcol Ex)。この方法では、12日齢の雌マウスから二次卵胞を採取して、卵胞内の成長期卵にsiRNAを顕微注入します。この卵胞を12日間体外培養することで卵を成長させ、体外成熟、体外受精することで受精卵を得ます。siRNA注入から受精まで2週間もの時間を与えられるので、多くの母性因子はこの方法でノックダウンできます。siRNAが2週間も安定的に機能できるのは、卵が非分裂細胞であるため細胞分裂による希釈が起こらないことが一因だと思います。この方法は過去に、NPM2やHIRAなどの安定な母性因子に対して用いました(Inoue and Aoki, 2010 FASEB J; Inoue and Zhang, 2014 NSMB)。



